| 释义 |
| 元素 名称 | | 元素符号 | | 原子 序数 | | 相对原子质量 (12C = 12.0000) | | | 英文名称 | |
| 原 子 结 构 | | 原子半径/Å: 1.46 原子体积/cm3/mol: 12.1 共价半径/Å: 1.11 电子构型: 1s2 2s2p6 3s2p2 离子半径/Å: 0.4 氧化态: 4 | 电子模型 | 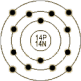 | |
| 发 现 | | 1824 在瑞典,斯德哥尔摩, 由 J.J. Berzelius 发现。 | |
| 来 源 | | 硅是第二个最丰富的元素,在地可中含25%,是构成粘土、沙、花岗岩和石英的主要成分。 | 用途 | 用于制造玻璃,太阳能电池,水泥和半导体等等。 | |
| 物 理 性 质 | | 状态:硬的深灰色非金属。 熔 点(℃):1410 沸 点(℃): 2355 密度(g/cc,300K): 2.33 比 热/J/gK : 0.71 蒸发热/KJ/mol : 384.22 熔化热/KJ/mol: 50.55 导电率/106/cm :2.52E-12 导热系数/W/cmK: 1.48 | |
| 地 质 数 据 | | 丰 度 滞留时间/年: 30 000 太阳(相对于 H=1×1012):4.47 × 107 海水中/p.p.m. 地壳/p.p.m.: 277 100 大西洋表面: 0.03 太平洋表面: 0.03 大西洋深处: 0.82 太平洋深处: 4.09 | |
| 生 物 数 据 | | 人体中含量 肝/p.p.m.: 12 - 120 器官中: 肌肉/p.p.m.: 100 - 200 血/mg dm-3 : 3.9 日摄入量/mg: 18 - 1200 骨/p.p.m.: 17 人(70Kg)均体内总量/g: c. 1 | |
|